من الطرق الممكنة لمهاجمة الخلايا السرطانية هي مهاجمتها بتيار كهربائي متردد منخفض الكثافة. يتدخل التيار الكهربائي في تدفق أيونات الكالسيوم والبوتاسيوم إلى الخلية ومنها، وهي عملية مهمة يؤدي اعتراضها إلى قتل الخلية.
لكن لهذا العلاج مشكلة، فالخلايا الصحية سوف تتعرض بدورها لاعتراض تدفق الأيونات، كما سيحدث للخلايا المسرطنة، لذا فهذا العلاج يقتل الخلايا السليمة والمسرطنة معاً. المطلوب هو طريقة لتركيز على العلاج على الخلايا السرطانية دون الخلايا السليمة.
وهنا يأتي دور أتيليو مارينو من المعهد الإيطالي للتكنولوجيا، وإنريك ألميتشي من جامعة تورين للتكنولوجيا وزملاء آخرين من إيطاليا. فقد استخدم هؤلاء الباحثون جزيئات نانو تولّد تياراً داخل الجسم لدى ضغطها بالموجات فوق الصوتية (ألترا-ساوند)، وتسمى هذه التقنية "الكهرضغطية". وقاموا بتحصيل أول أدلة على إمكانية تحويل هذا الأسلوب إلى علاج ناجح للسرطان.
يعتبر هذا العلاج مباشراً وسليماً ولا غبار عليه من الناحية النظرية. فالمواد الكهرضغطية تولد شحنة لدى ضغطها (وبالمثل فهي تغير شكلها لدى توجيه صعقة كهربية إليها). وهي تستخدم كثيراً في أغراض كثيرة، من الميكروفون إلى المُحرك الكهربائي.
فكرة مارينو وزملاؤه تتلخص في حقن جزيئات نانو في الجسم ثم قصفها بالموجات فوق الصوتية. ومن شأن الضغط العالي والمنخفض المرتبط بالموجات فوق الصوتية أن يؤدي بالجزيئات النانو إلى توليد شحنات تتعارض مع القنوات الأيونية للخلايا ويقتلها. وقد اختار الفريق جزيئات نانو من مركب الباريوم-تيتانيت، ويعتبر جزيء قابل للاستخدام داخل الجسم البشري بما أنه يخلو من مادة الرصاص.
كما طوّر الفريق آلية هامة للاستهداف. فالجزيئات النانو يجب أن تُصمم بحيث تلتصق بالخلايا المسرطنة مع تجاهلها الخلايا السليمة. وقد أنجز مارينو وزملاؤه هذه المهمة عن طريق تغليف جزيئات النانو ببوليمر بلاستيك، ثم وضع هذا المُركّب داخل أجسام مضادة تلتصق بمستقبلات موجودة في نوع بعينه من الخلايا السرطانية.
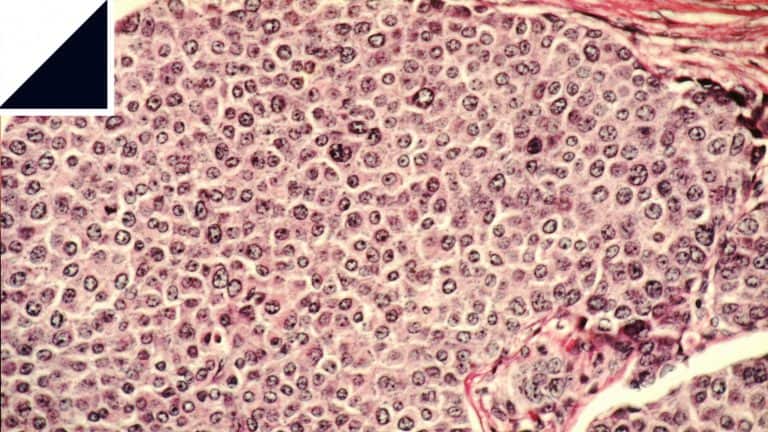
وفي هذه الحالة قام الفريق بالتركيز على النوع الشرس من خلايا سرطان الدماغ، المُسمى "غليوبلاستوما مالتيفورم" (glioblastoma multiforme). وفي أغشية هذه الخلايا مُستقبلات "ترانسفيرين"، على النقيض من أغلب الخلايا السليمة. لذا قام الفريق بتغليف الجزيئات النانو بغشاء من أجسام الترانسفيرين المضادة، التي تلتصق بمستقبلات الترانسفيرين على الخلايا المسرطنة. ويؤدي هذا إلى تحويل الجزيئات النانو إلى صواريخ موجهة لا تستهدف إلا الخلايا السرطانية. ويجب أن تمر الجزيئات الانو أيضاً عبر عائق خلايا دم المخ، وهو عامل مهم في علاج سرطانالدماغ. يمكن للجزيئات النانو إنجاز هذا الأمر إذا كانت صغيرة بالقدر الكافي. لذا اختار الفريق جزيئات يبلغ نصف قُطرها 300 نانو-متر، وهو الحجم القادر على تجاوز هذا العائق.
اختبر مارينو وزملاؤه هذه الطريقة حيث قاموا معملياً بتكوين خلايا أورام في المخ مصحوبة بعائق يحاكي ذلك الخاص بعائق خلايا دم المخ. ثم قام الباحثون بقياس مدى نجاح الجزيئات النانو في اختراق ذلك العائق. وبعد هذا قاموا بقصف عينات خلايا المخ بالموجات فوق الصوتية مع استخدام علاج كيميائي للسرطان يُدعى "تيموزولوميد".
يقول الفريق إن الجزيئات النانو تمكنت من اختراق الخلايا السرطانية بسهولة نسبية، وأن الجزيئات عندما دخلت الخلايا السرطانية وقصفتها بالموجات فوق الصوتية، تحسنت كثيراً فعالية العلاج الكيميائي، "تيموزولوميد".
يُظهر استخدام العلاجين الكيميائي والكهروفيزيائي معاً قدرة مبشرة على تحسين علاج سرطانالدماغ. وقال مارينو وفريقه: "أدى التحفيز الكهروضغطي بالتزامن مع تركيز غير سام من التيموزولوميد إلى زيادة الحساسية والاستجابة للعلاج الكيميائي وإلى كفاءة عالية في التخلص من الخلايا المسرطنة". لكن هناك مشكلات يجب التغلب عليها قبل النظر إلى هذه الطريقة كعلاج فعال محتمل. فالنموذج الذي استخدمه مارينو ورفاقه أبسط بكثير من الظروف الحقيقية داخل الجسم. ويخطط الفريق لاختبار نماذج أكثر تعقيداً بكثير واختبار فعالية العلاج داخل جسم المريض. كما يخططون للبحث عن جزيئات نانو بأحجام وأشكال تسمح بتحسين السيطرة على آثار التقنية الكهروضغطية.
لهذه التقنية قدرة على النجاح، لا سيما في استهداف مخلفات الأورام الميكروسكوبية التي تعد العامل الرئيسي للانتكاس وعودة الورم السرطاني بعد إجراء الجراحة. وربما كان الطريق ما زال طويلاً للوصول لعلاج نهائي، لكن هذا النوع من الأبحاث النانو-طبية يبدو مُبشراً للغاية.